В данной работе я хотел поговорить о ставшей модной сейчас теме: о стволовых клетках (СК). Разговор о них был затронут мной еще в предыдущем докладе [1]. Да и в других докладах в МОИПе это также обсуждалось. Сейчас хочется подвести некоторые предварительные итоги, внести некий оптимизм в геронтологию. Ранее мной затрагивалась тема: как можно увеличить продолжительность жизни (ПЖ) человека до 1,5-2 раз уже в настоящее время, используя известные способы и учитывая их эффективность на основе анализа данных, полученных разным способом. Были проанализированы данные экспериментов на лабораторных животных, ПЖ животных в природе, результаты исследований, проведенных с использованием клеточных моделей, а также результаты теоретических исследований [2]. Здесь мы продолжим тему возможности большого (в 2-3 и более раз) увеличения ПЖ человека с использованием клеточной терапии, обсуждение которой было начато в предыдущей статье [1].
Прежде всего хочу поблагодарить В.Е. Чернилевского, который наконец-то подарил мне свою очень подробную статью о СК [3]. До того, как он сделал эту работу, мы с ним подолгу беседовали на эту тему, а именно о роли СК в старении, о возможности их использования для увеличения ПЖ человека, о пролиферативном потенциале этих клеток.
В работе В.Е. Чернилевский [3] очень подробно изложил биологию СК, применение, изменение СК в стареющем организме, возможности замедления старения, возможности продления жизни. Для общего представления о СК можно сделать следующую приблизительную их классификацию, указать распределение СК в организме и перечислить их основные функции.
Считается, что существует несколько сотен типов клеток [4, 6]. Их можно разбить на группы:
- тотипотентные эмбриональные СК (зигота и бластомеры);
- плюропотентные эмбриональные СК (на стадии гаструлы дают начало всем типам СК эмбриона и взрослого организма, в том числе половым клеткам, в них имеется высокий уровень теломеразной активности).
- монопотентные стволовые клетки дают начало одному типу клеток, например, кроветворные клетки производят эритроциты, моноциты и т.д. Такая клетка считается материнской дифференцированной стволовой клеткой;
- мультипотентные стволовые клетки дают начало широкому спектру клеток.
При этом различают симметричное и ассимитричное деление СК.
При симметричном делении клетки производят себе подобные клетки и не имеют соответствующую специализацию.
При ассимитричном делении одна клетка остается стволовой, а другая становится родоначальником линии с ограниченным пролиферативным потенциалом. Последние называются прогениторными клетками, которые дифференцируются в одном или в нескольких направлениях. Прогениторные клетки дают начало монопотентным клеткам предшественникам - клеткам тканей тела.
Все типы стволовых и прогениторных клеток, а также клеток предшественников однородны в большинстве тканей организма, в том числе в головном мозге, поэтому их трудно идентифицировать по внешним признакам.
СК различаются по пролиферативной способности. Быстрообновляющиеся СК - клетки, которые производят клетки крови, кишечного эпителия, эпидермиса и др. Медленно обновляющиеся СК - производят хондроциты, гепатоциты и др. Малообновляющиеся СК - нейроны, миоциты, тучные клетки.
Основной источник СК - костный мозг, однако стволовые клетки имеются и в других тканях, например, в головном мозгу, кишечном эпителии, печени, мышцах, коже [3,4]. Часть СК костного мозга являются гемопоэтическими и производят все клетки крови, другая часть является стромальными или (другое название) мезенхимальными, которые могут давать начало клеткам, образующим ткани костей, хряща, мышц, связок, эпителия кожи или внутренних органов, образовывать гепатоциты, кардиомиециты, нервные, и эндотелиальные клетки [3, 5].
Нет однозначного мнения о роли и возможностях СК, но несмотря на это работа активно ведется и в России и в других странах. Некоторые исследователи, например В.Е. Чернилевский, достаточно категоричны и отвергают связь СК со старением. Считается, что их роль заключается в поддержании определенных систем организма, а к старению они не имеют никакого отношения, т.е., СК сами по себе, а старение организма само по себе, и СК не могут влиять на процесс старения.
Следует заметить, однако, что есть обратное взаимодействие между старением и СК. Иначе говоря, старение влияет на СК, ухудшает их свойства, ограничивает их пролиферативные возможности, вызывает их гибель, что приводит к уменьшению числа живых СК в тканях и органах.
Имеет смысл процитировать выводы В.Е. Чернилевского, проведшего большую работу по анализу функций СК в организме [3]. «СК не имеют внутренней причины старения, выполняют свою функцию по самообновлению организма до конца жизни и противодействуют старению. Под влиянием возрастного изменения микроокружения СК в стареющем организме изменяются и функции СК. Использование последних достижений в изучении СК позволяет эффективно корректировать возрастные изменения организма с помощью клеточной терапии и увеличить среднюю ПЖ человека до индивидуального предельного срока.
Дальнейшее увеличение максимальной ПЖ возможно при воздействии на старение организма, причиной которого не являются СК. В ряду поколений организмов СК ответственны как за бесполое, так и половое размножение, т.е. в филогенезе наблюдается непрерывность линий половых и СК, что обеспечивает бессмертие жизни на Земле. Для продления жизни млекопитающих и человека необходимо замедлять старение. В настоящее время единственным способом замедления старения и продления жизни человека представляется создание периодического замедления обмена веществ, гипобиоза, с помощью комплекса специальных тренировок»
Из процитированного абзаца видна очевидная безысходность применения СК для борьбы со старением, точнее невозможность повлиять на максимальную длительность жизни. Победить старение невозможно, увеличить ПЖ организма радикально нельзя!
С некоторыми выводами автора можно согласиться. Но мне хотелось быть более оптимистичным и не согласиться с тем категоричным утверждением автора, что нельзя применить СК для решения проблем старения. На мой взгляд, обновление органов - это и есть омоложение и есть борьба со старением. Если обновить (омолодить) все органы и ткани организма, то и весь организм станет обновленным (молодым), а это и есть победа над старостью.
Мне представляется, что на этом пути (использования СК для омоложения органов и всего организма) требуется решение ряда технических, биологических и медицинских проблем. Однако, кроме названных проблем есть и формальные, в частности, к использованию СК осторожно относится Минздрав РФ. В США использование СК вообще запрещено. Однако в России отсутствие прямого запрещения применения СК в медицине воспринимается по принципу «Что не запрещено, то разрешено», поэтому уже несколько десятилетий СК используют для «лечения» заболеваний некоторых органов и для косметического «омоложения». Причем об этом можно узнать в основном из периодической печати или сообщений разных информационных агенств. В серьезных научных публикациях сообщения на тему действительных результатов лечения или омоложения людей очень редки и осторожны .
Хотелось бы внести определенную ясность в то, каковы все-же перспективы использования СК.
Если исходить из отрывочных сведений о применении СК, то можно прийти к выводу, что нет фактических свидетельств реального омоложения или увеличения ПЖ людей. Поскольку все же терапия СК проводится, то почему же нет реальных достижений?
На этот счет у нас есть определенные предположения. Используя результаты наших экспериментов и данные литературы мы пришли к следующему заключению. Поскольку СК присутствуют в организме, но они не обновляют старящиеся клетки органов и тканей, значит дело не только в них. Ввод же СК в организм видимо обновляют некоторые органы и ткани, но все же нет сведений о влиянии СК на ПЖ человека или на его здоровье. В своих многолетних исследованиях на культурах клеток животных и человека мы обнаружили одно очень важное обстоятельство, которое может объяснить, почему нет однозначных успехов при терапии стволовыми клетками.
Мы обнаружили, что даже молодые и здоровые клетки, способные к быстрой пролиферации, не могут долго выживать в окружении старых, неделящихся клеток [7].
Это открытие было сделано нами в экспериментах, выполненных на культивируемых клетках, в частности, на трансформированных клетках китайского хомячка, раковых клетках человека линии HeLa и эмбриональных диплоидных фибробластах человека. При обычной для нас постановке опыта, т.е. при условии, что культура клеток растет в культуральных флаконах без пересева и без периодической замены ростовой среды на свежую в течение всего времени эксперимента (примерно 1-1,5 мес.), после достижения клетками монослоя (насыщающей плотности) большинство клеток перестает делиться и начинает гибнуть. При этом часть клеток в монослое остается еще какое-то время живой. Со временем все большее число клеток в культуре становятся мертвыми и неспособными к делению и в конце - концов все клетки гибнут. Если в момент достижения монослоя и далее, периодически, например, 1 раз в неделю производить замену старой ростовой среды на свежую, но не делать пересева клеток в чистый флакон, то в этом случае может наблюдаться разная судьба культур, в зависимости от условий культивирования. Как выяснилось, эта разница будет иметь место при использовании разного материала, на котором растут клетки. Оказалось, что если они растут в пластмассовых флаконах или пластмассовых планшетах без пересева - результат один - клетки долго не выживают, хотя производится периодическая замена среды на свежую. Т.е. постоянное присутствие свежей полноценной среды еще не гарантирует неограниченной ПЖ культуры, растущей на пластмассовой поверхности. Иногда клетки в периодически заменяемой среде могут жить лишь немного дольше, чем без замены среды, но все равно гибнут. Клетки все равно погибнут если среду периодически менять на свежую сколько угодно раз.
Иная картина наблюдается если клетки растут на другой поверхности, но не на пластмассовой, а на стеклянной - на дне стеклянных флаконов Карреля. Оказывается, в этом случае культура клеток может жить в десятки раз дольше (более 20 раз), чем на пластмассовой поверхности или в контроле на стекле, но без замены среды. Такое 20-кратное увеличение ПЖ культур практически означает их потенциальную неограниченную ПЖ. Необходимым условием является стеклянная ростовая поверхность и периодическая (например, 1 раз в неделю) замена ростовой среды на свежую. При этом именно на стеклянной поверхности и при этих условиях клетки могут жить (делиться) в культуральных флаконах без пересева практически неограниченно долго.
Почему же имеется такая разница по ПЖ культур, живущих на стекле и на пластмассе? Чем стекло оказывается «лучше», чем пластмасса, для выживания культур клеток во времени?
Чуть ниже мы вернемся к обсуждению этого вопроса. Сейчас рассмотрим результаты некоторых конкретных экспериментов. На рис. 1 показано изменение числа живых клеток, растущих в пластмассовых планшетах. Площадь лунки 2 см2. В эксперименте использовали трансформированные клетки китайского хомячка линии линия B11dii - FAF28 (клон 237, полученные из яичников взрослой самки китайского хомячка и претерпели спонтанную трансформацию) и раковые клетки человека линии HeLa. Эти клетки не имеют ограничений по числу делений, если их периодически пересевать в новую ростовую среду. В наших условиях культуры росли без пересева в ростовой среде Игла (МЕМ) с 10% сыворотки крупного рогатого скота. Использовали по 3 лунки на каждый вид экспериментальной культуры. Подсчет клеток проводили непосредственно на ростовой поверхности с использованием инвертированного микроскопа при увеличении 120.
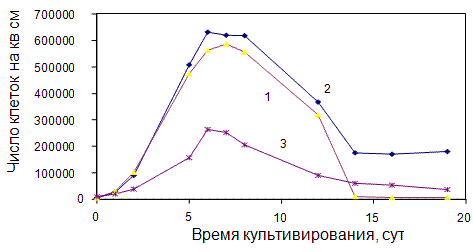
Рис.1. Изменение числа трансформированных клеток китайского хомячка (1,2) и клеток HeLa (3), растущих в пластмассовых планшетах (состав атмосферы постоянный) при периодической замене среды на свежую (2,3) и без замены (1).

Рис.2. Изменение числа трансформированных клеток китайского хомячка, растущих в пластмассовых планшетах (состав атмосферы постоянный) при периодической замене среды на свежую (2) и без замены (1).
Кривая 1 на рис.1 отражает изменение числа живых трансформированных клеток китайского хомячка без замены ростовой среды на свежую, кривая 2 - изменение числа таких же клеток, но при периодической смене среды, начиная с момента достижения монослоя (замену проводили 1 раз в 3-4 дня), кривая 3 - число живых клеток HeLa также с заменой среды (аналогично предыдущему).
Из рисунка 1 видно, что во всех трех случаях культуры после достижения монослоя постепенно гибнут. Число живых клеток уменьшается, несмотря на периодическую замену ростовых сред на свежие.
Такая же картина наблюдалась в другом аналогичном эксперименте, что отражено на рис. 2. Хорошо видно, что обе культуры гибнут как без замены среды (кривая 1), так и при периодической замене среды (кривая 2). Единственное отличие кривых в том, что с заменой среды клетки растут немного дольше, достигают большего числа и живут немного дольше, чем в культуре без замены среды.
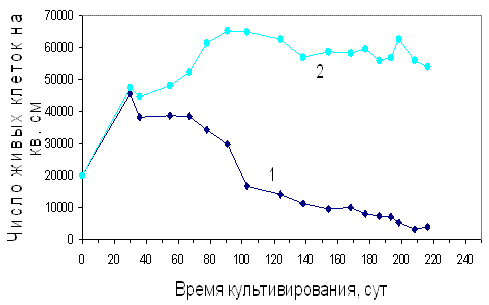
Рис.3. Изменение числа эмбриональных диплоидных фибробластов человека, растущих в негерметичных пластмассовых флаконах (состав атмосферы постоянный) при периодической замене (2) и без замены (1) среды на свежую [7].
Если среда не меняется, то питательные вещества постепенно расходуются и на поздней стационарной стадии их недостаток может сказываться на способности клеток к делению. Периодическая замена сред означает, что в ростовой среде много питательных веществ и ростовых факторов для поддержания жизни клеток, но это не спасает клетки от гибели. Что же вызывает гибель клеток?
В другом эксперименте (рис. 3) наблюдали изменение числа эмбриональных диплоидных фибробластов человека, растущих в негерметичных пластмассовых флаконах (состав атмосферы постоянный при содержании 5-7% СО2) при периодической замене (кривая 2) и без замены (кривая 1) ростовой среды на свежую. Клетки росли в среде ДМЕМ (с 40 мкг/мл гентамицина) c 10% эмбриональной телячьей сыворотки. Замену сред во флаконах с фибробластами производили с интервалом 3-5 суток в первые 3 мес. и 7-9 суток - в последующие месяцы. Видно, что замена среды меняет характеристики выживания клеток. ПЖ культур эмбриональных диплоидных фибробластов человека в условиях периодической замены среды незначительно возрастает, но при осмотре культуры выясняется, что клетки не делятся, постепенно деградируют и культура не обновляется.
И хотя их видимое число большое, но на самом деле это не живые, а мертвые клетки. В связи с этим такие культуры также не могут существовать неограниченное время [7].
Однако существуют все же такие условия, при которых может быть практически бесконечная ПЖ культур. Это видно из нескольких экспериментов, описанных ниже.
В одном из экспериментов трансформированные клетки китайского хомячка жили в культуре без пересева и без замены среды менее 1 мес, а при периодической замене среды - более 6 мес, т.е. в 6 раз больще, чем в контроле (рис.4) и также примерно в 6 раз дольше, чем в экспериментах, показанных на рис. 1 и 2. Отличие данного эксперимента от предыдущих состояло только в том, клетки росли не на пластмассовой поверхности, а на стекле - на дне стеклянных флаконов Карреля (площадь флакона 23 см2). Для роста использовали ту же среду Игла с 10% сыворотки крупного рогатого скота. Т.о. ПЖ культуры на стеклянной поверхности при периодической замене среды была гораздо выше, чем без замены среды [7].
Другой эксперимент длится уже более 2-х лет и продолжается в настоящее время, а результат эксперимента еще более впечатляющий - клетки живут при тех же условиях больше, чем в 20 раз (рис. 5). Используются также трансформированные клетки китайского хомячка. Культуры клеток растут в стеклянных закрытых герметично флаконах Карреля площадью 23 см2 в питательной среде Игла с 10% сыворотки крупного рогатого скота. Кривая 1 показывает изменение числа живых клеток в контрольной культуре без замены среды и без пересева. Кривая 2 - изменение числа живых клеток в опыте без пересева, но с периодической (1 раз в 5-7 сут) заменой среды на свежую. Видно, что ПЖ контрольной культуры не превышает 35 сут. Напротив, в опыте ПЖ культуры несоизмеримо выше - более 800 сут, т.е более 2-х лет и 2-х мес, что почти в 23 раза превышает жизнь культуры в контроле.
Т.о. видно, что культуры трансформированных клеток в стеклянных флаконах могут существовать неопределенно долгое время, а вот в пластмассовых флаконах или в планшетах не могут. Почему? Визуальное наблюдение за клетками показало в чем отличие тех и других культур. Оказалось, что на пластмассовой поверхности клетки постоянно прикреплены к ней. Причем они как правило находятся на ней и тогда, когда погибают или уже будучи мертвыми и не способными к делению. Они не открепляются от ростовой поверхности и мешают делиться молодым клеткам. Не имея возможности делиться молодые клетки лежат, постепенно стареют и потом погибают.
На стеклянной поверхности наблюдается другая картина. Как правило, старые, погибающие клетки, а тем более мертвые клетки округляются, прекращают распластываться, не могут удержаться на стекле и переходят в ростовую среду (всплывают, перекатываются по ростовой поверхности при покачивании флаконов). Это отличие и является определяющим. Именно это и позволяет объяснить, почему на стеклянной поверхности культуры клеток могут жить без пересева, но при периодической замене среды неограниченное время. Это происходит из-за того, что старые клетки отмирают, открепляются от ростовой поверхности и освобождают место молодым, способным делиться клеткам. Молодые клетки начинают делиться и дочерние клетки заполняют открывшиеся пространства.

Рис.4. Изменение числа трансформированных клеток китайского хомячка, растущих в стеклянных герметично закрытых флаконах при периодической замене среды на свежую (2) и без замены (1) [7].

Рис. 5. Изменение числа живых трансформированных клеток китайского хомячка, растущих в негерметичных пластмассовых флаконах (состав атмосферы постоянный) при периодической замене (2) и без замены (1) среды на свежую.
В последующем такие старые, открепившиеся от ростовой поверхности клетки, устраняются из флакона вместе со старой средой, при замене на свежую.
При этом из флакона устраняются и токсичные продукты распада погибших клеток, что также обеспечивает живым клеткам возможность делиться. Затем молодые клетки аналогично стареют, гибнут, потом открепляются от стекла и освобождают место для роста способных к делению молодых клеток. Процесс может повторяться неограниченное время, благодаря чему клетки в культуре все время обновляются и вся культура остается живой в течение неограниченного времени. В отличие от ситуации, характерной для нахождения клеток на стеклянной поверхности, при росте клеток на пластмассовой поверхности старые клетки не открепляются от нее, поэтому молодые, способные к делению клетки не имеют возможности делиться, т.к. нет пространства для деления (им мешают неоткрепившиеся старые клетки) и культура не обновляется. В результате все молодые клетки в таких культурах постепенно стареют, гибнут и, соответственно, гибнет вся культура.
Похожая картина может наблюдаться и в организме. Даже если в органах есть много молодых, способных к делению клеток (в том числе стволовых), но если есть и старые клетки, которые не удаляются из органа, тогда молодые клетки (в т.ч. стволовые) не могут поделиться из-за отсутствия места для деления и не могут заменить молодыми дочерними клетками эти старые нефункционирующие клетки. В результате клетки в органе не обновляются, все большее число клеток гибнет, а орган, состоящий из старых, плохо работающих клеток, или вообще не работающих, также сам становится плохо работающим и в конце - концов перестает выполнять необходимые функции. Отказ работы одного органа может вызвать ухудшение работы других органов организма. Плохая работа органов отрицательно сказывается на жизнеспособности всего организма и может привести к его гибели. По этой же причине, вероятно, нет успехов в лечении болезни Альцгеймера или подобных когда использовали имплантацию в мозг эмбриональных клеток. По нашему мнению эмбриональные клетки не делиться из-за недостатка места, занятого старыми клетками.
Все же попытки лечения разных заболеваний стволовыми или эмбриональными клетками предпринимаются постоянно. Клеточные трансплантации осуществляются при лечении болезней сосудов (инсульт, инфаркт миокарда, хроническая сердечная недостаточность, вегетососудистая дистония и др.), при поражении центральной нервной системы, болезни Альцгеймера и Паркинсона, заболевании крови (в т.ч. анемии), болезнях печени и почек, сделаны попытки лечения иммунодифицитных состояний, рассеянного склероза, онкологических заболеваний, сахарного диабета, пороков развития [3, 8, 9, 10, 11, 12]. Установлено, что имплантация стромальных СК в искусственно поврежденные ткани животных приводит к восстановлению этих тканей. Таким образом удавалось восстанавливать нервные клетки, кардиомиоциты, эндотелий, гепатоциты. Считается, что СК костного мозга могут транспортироваться через кровоток в другие ткани и давать начало клеткам соответствующего фенотипа. Такие СК были обнаружены в крови больных с первичной гиперлипедимией и ишемической болезнью сердца и предполагается, что атеросклероз и проникновение клеток из костного мозга как-то могут быть связаны, т.к. на стенках больных сосудов обнаруживаются скопления из гемопоэтических и стромальных клеток. При чем, стромальные СК присутствуют у людей с ишемической болезнью сердца и их нет у здоровых.
Это может означать, что СК мобилизуются в костном мозге из-за атеросклероза и транспортируются в места повреждений сосудов (5). Однако использование клеточной терапии пока не приносит массовых успехов, а оптимизм зиждется на предположениях и предварительных результатах. Мы полагаем, что больших успехов на этом пути можно будет добиться, если учитывать открытые нами особенности поведения молодых клеток в окружении старых клеток. Таким образом, напрашивается вывод, чтобы стволовые клетки нормально работали и обновляли популяцию клеток органа или ткани, нужно найти способ удаления из органа или ткани старых, не функционирующих клеток. Механизм разрушения клеток в старом организме по механизму апоптоза естественным образом видимо также не работает. Но было бы неплохо попробовать запустить его искусственным способом. Для удаления старых клеток можно было бы попробовать применять некоторые ферменты, которые способны разрушать мембраны клеток. В частности, это мог бы быть фермент трипсин, точнее растворы трипсина,
Автор выражает благодарность А.Н. Хохлову за предоставление культур клеток, помощь в планировании и проведении некоторых экспериментов.
См. подраздел  Литература.
Литература.
 Обсудить на форуме
Обсудить на форуме






